Điều mà không có công ty máy tạo nhịp (và máy phá rung, máy điều trị suy tim) nào phủ nhận là Cty Biotronik là công ty đã đạt mức an toàn cao nhất, đã không có bất cứ FDA recall nào trong vòng 10 năm nay. Trong thời gian này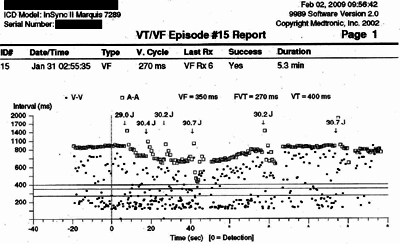 Cty Medtronic năm 2007 bị cơ quan FDA (USA) ra lệnh recall (thu hồi) dây sốc Sprint Fidelis đã tạo đau đớn tận cùng cho một số khá lớn BN, kể cả một số BN ở VN. Hình bên phải (từ BS Ip, Michigan State U) là quá trình nhịp được máy phát hiện vì dây sốc hư đã đưa đến BN bị 6 sốc liên tục, số sốc điều trị tồi đa cho một cơn loạn nhịp trong các máy phá rung Medtronic. Hiện nay mức dây hư cần phải thay để tránh bị bão sốc lầm từ 16% (trung bình) đến 37%.Kế đến Cty St Jude đã phải recall dây sốc Riata, Riata ST năm 2011, dây Cty Medtronic năm 2007 bị cơ quan FDA (USA) ra lệnh recall (thu hồi) dây sốc Sprint Fidelis đã tạo đau đớn tận cùng cho một số khá lớn BN, kể cả một số BN ở VN. Hình bên phải (từ BS Ip, Michigan State U) là quá trình nhịp được máy phát hiện vì dây sốc hư đã đưa đến BN bị 6 sốc liên tục, số sốc điều trị tồi đa cho một cơn loạn nhịp trong các máy phá rung Medtronic. Hiện nay mức dây hư cần phải thay để tránh bị bão sốc lầm từ 16% (trung bình) đến 37%.Kế đến Cty St Jude đã phải recall dây sốc Riata, Riata ST năm 2011, dây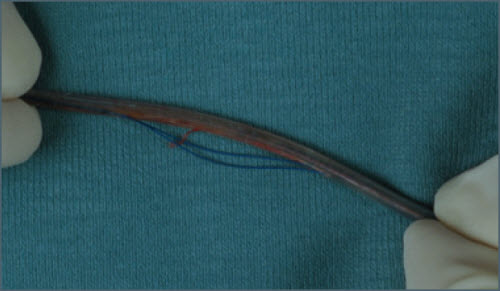 thất trái QuickFlex và QuickSite năm 2012, tất cả vì sự cố dây đồng lòi ra. Dây điện cực sôc Riata của Cty St Jude có sự cố dây đồng lòi ra với mức sự cố >24%. Tuy nhiên cơ quan FDA cũng đã quan tâm và đặc biệt khuyên các BN cần phải kiẻm tra tình trạng dây với x-quang. Cho đến nay cách giải quyết các dây điện cực này vẫn chưa được thống nhất. Dây Durata, đã thay thế Riata, là đề tài bàn cải sôi nỗi ở tất cả các hội nghị tim mạch lớn, trừ ở VN, về an toàn lâu dài. Ngoài các recall nghiêm trọng trên, các công ty Medtronic và St Jude cũng đã có nhiều recall class II các máy điều trị nhịp tim và dây điện cực khác (xem tóm tắt).Cũng trong thời gian này cả 2 công ty Medtronic và St Jude đều đã bị FDA gửi thư cảnh cáo về quy trình thiết kế các thiết bị. Cty Medtronic bị thử cảnh cáo năm 2009.Thư cảnh cáo mới nhất đã được gửi đến Cty St Jude tháng 10, 2012, và nêu lên các khiếm khuyết trong giai đoạn phê chuẩn thiết kế (design validation) dây sốc Durata. Với các khiếm khuyết này, làm sao Cty St Jude có thể tuyên bố là dây sốc Durata an toàn?Trong cả thời gian này, Cty Biotronik đã không có recall hoặc nhận thư cảnh cáo nào hết!Trong khi máy tạo nhịp/phá rung chỉ có thời gian hoạt động 5-15 năm, dây điện cực có thể ở trong người bạn 20-30 năm. Nếu dây có sự cố, thì ở VN chỉ có thể bỏ dây lại trong người và thêm dây khác. Nhưng, tĩnh mạch của con người đâu có phải rộng thênh thang, muốn cấy vào bao nhiêu dây điện cực cũng được? Đã có nhiều BN khi thay máy đã phải thay vai cấy máy, vì khi tháo máy ra, thì BS phát hiện dây điện cực không thể sử dụng lại được (khi dây bị động thì hư), và tĩnh mạch đã hẹp lại nên không thể đưa dây mới qua. Ở Âu-Mỹ, khi dây hư thì có thể đến BS chuyên môn rút dây, để lấy dây điện cực ra. Thủ thuật này có mức sự cố nhỏ, nhưng không phải 0. Ngay cả ở các trung tâm nhiều kinh nghiệm mức sự cố là 1,4%, mức tử vong là 0,28%! Đây là lý do nhiều dây Riata đã bị sự cố dây đồng lòi ra trong tĩnh mạch, mà BS vẫn do dự không rút ra. Tuy nhiên đén khi dây bị hư về phương diện điện (sốc lầm, có nhiễu, dây đồng đứt) thì BS sẽ phải cấy dây mới. thất trái QuickFlex và QuickSite năm 2012, tất cả vì sự cố dây đồng lòi ra. Dây điện cực sôc Riata của Cty St Jude có sự cố dây đồng lòi ra với mức sự cố >24%. Tuy nhiên cơ quan FDA cũng đã quan tâm và đặc biệt khuyên các BN cần phải kiẻm tra tình trạng dây với x-quang. Cho đến nay cách giải quyết các dây điện cực này vẫn chưa được thống nhất. Dây Durata, đã thay thế Riata, là đề tài bàn cải sôi nỗi ở tất cả các hội nghị tim mạch lớn, trừ ở VN, về an toàn lâu dài. Ngoài các recall nghiêm trọng trên, các công ty Medtronic và St Jude cũng đã có nhiều recall class II các máy điều trị nhịp tim và dây điện cực khác (xem tóm tắt).Cũng trong thời gian này cả 2 công ty Medtronic và St Jude đều đã bị FDA gửi thư cảnh cáo về quy trình thiết kế các thiết bị. Cty Medtronic bị thử cảnh cáo năm 2009.Thư cảnh cáo mới nhất đã được gửi đến Cty St Jude tháng 10, 2012, và nêu lên các khiếm khuyết trong giai đoạn phê chuẩn thiết kế (design validation) dây sốc Durata. Với các khiếm khuyết này, làm sao Cty St Jude có thể tuyên bố là dây sốc Durata an toàn?Trong cả thời gian này, Cty Biotronik đã không có recall hoặc nhận thư cảnh cáo nào hết!Trong khi máy tạo nhịp/phá rung chỉ có thời gian hoạt động 5-15 năm, dây điện cực có thể ở trong người bạn 20-30 năm. Nếu dây có sự cố, thì ở VN chỉ có thể bỏ dây lại trong người và thêm dây khác. Nhưng, tĩnh mạch của con người đâu có phải rộng thênh thang, muốn cấy vào bao nhiêu dây điện cực cũng được? Đã có nhiều BN khi thay máy đã phải thay vai cấy máy, vì khi tháo máy ra, thì BS phát hiện dây điện cực không thể sử dụng lại được (khi dây bị động thì hư), và tĩnh mạch đã hẹp lại nên không thể đưa dây mới qua. Ở Âu-Mỹ, khi dây hư thì có thể đến BS chuyên môn rút dây, để lấy dây điện cực ra. Thủ thuật này có mức sự cố nhỏ, nhưng không phải 0. Ngay cả ở các trung tâm nhiều kinh nghiệm mức sự cố là 1,4%, mức tử vong là 0,28%! Đây là lý do nhiều dây Riata đã bị sự cố dây đồng lòi ra trong tĩnh mạch, mà BS vẫn do dự không rút ra. Tuy nhiên đén khi dây bị hư về phương diện điện (sốc lầm, có nhiễu, dây đồng đứt) thì BS sẽ phải cấy dây mới. |
Về phương diện an toàn dây điện cực thì
- Trong quá trình hoạt động từ năm 1963 đến nay (12/2013), >50 năm, chỉ có Cty Biotronik là duy nhất đã không có bất cứ recall dây điện cực nào cả! Con số KHÔNG, zero, nada, …!
Đã có nhiều giải thích tình trạng “bất thường” 0 recall của Cty Biotronik, như dưới đây
- Cty Biotronik có trụ sở ở Âu-Châu nên không chịu sự giám sát của FDA.
- Vì có cung cấp máy vào thị trường Mỹ, nên Cty Biotronik phải chịu sự kiểm soát của FDA như Cty Medtronic, St Jude. Hàng năm thanh tra FDA có đến trụ sở Biotronik ở Berlin, CHLB Đức, kiểm tra quy trình thiết kế và sãn xuất. Các Cty Medtronic và St Jude đều có cơ sở thiết kế và sãn xuất thiết bị ở ngoài Mỹ, cũng phải chịu các cuộc thanh tra tương tự.
- Các bạn được cấy bộ máy điều trị nhịp tim của Medtronic và St Jude có biết thật sự các thiết bị đó đã được thiết kế và sãn xuất ở đâu không? Không nhất thiết là từ Mỹ đâu! Ngoài ra còn có một số máy được thiết kế và sãn xuất riêng cho thị trường đệ tam thế giới, như máy tạo nhịp St Jude Sustain!
- Cty Biotronik có thị trường nhỏ nên các sự cố ở mức thấp
- Cty Biotronik năm 2011 có doanh số trên 1 tỷ Euro (>1,3 tỷ USD), mà >50% là từ các thiết bị điều trị nhịp tim. Đây không phải là một công ty với doanh số vài triệu USD đâu!
- Ngoài ra, doanh số về thiết bị điều trị nhịp tim của các Cty Medtronic và St Jude cũng không phải gấp 10 lần doanh số Cty Biotronik. Doanh thu năm 2011 thiết bị điều trị nhịp tim của Medtronic chỉ là 5 tỷ USD (tổng số doanh thu là 16 tỷ USD). Doanh thu thiết bị điều trị nhịp tim của Cty St Jude năm 2011 là 59% của 4,7 tỷ USD (=2,8 tỷ USD).
- Mà các cơ quan chức trách, như FDA, quan tâm về tất cả các sự cố. Thí dụ điển hình là Cty Telectronics, một Cty cùng thời với Biotronik, được thành lập năm 1963, đã bị xóa sổ năm 1996 chỉ vì vài BN tử vong do thiết kế sai lầm dây điện cực nhĩ. Công ty Guidant cũng bị xóa sổ sau khi có một vài BN đột tử năm 2005 do máy phá rung không phát sốc được khi cần do thiết kế không an toàn.
Lý do Cty Biotronik đạt được mức an toàn cao, thật ra rất đơn giản: truyền thống an toàn BN trên hết. Cty nào cũng có những tuyên bố tương tự. Chúng tôi xin được trình 2 thí dụ bên dưới để chứng minh truyền thống đó.
- Tác giả bài này nguyên là Phó Tổng Giám Đốc Kỹ thuật (Vice-President Engineering) của chi nhánh thiết kế và sãn xuất ở Mỹ của Cty Biotronik. Trong nhứng năm cuối thập niên 90. Tác giả đã làm việc trực tiếp với cố GS Max Schaldach (1936-2001), người sán lập Cty Biotronik. Từ năm 1993 đến 1998, Ts Thống đã là người lãnh đạo kỹ thuật nhóm thiết kế máy phá
 rung hai buồng đầu tiên của Cty Biotronik, máy Phylax AV. Ts Thống và một kỹ sư khác là tác giả chương trình Smart Detection phân biệt nguồn gớc các cơn loạn nhịp nhanh (thất hay trên thất) hiện vẫn còn được dùng chỉ với những thay đổi nhỏ so với chương trình nguyên thủy trong máy Phylax AV. Năm 1997, chương trình thiết kế máy Phylax AV đã kết thúc và Cty Biotronik sửa soạn xin cấp giấy phép lưu hành CE (Communauté Européenne). Các hoạt động thiết kế và phê chuẩn thiết kế (design validation) của nhóm kỹ sư ở Mỹ đã hoàn tất. Giai đoạn cuối cùng là phê chuẩn ở cấp Cty Biotronik. Ở giai đoạn này, các kỹ sư phê chuẩn thiết kế Đức tại Berlin khám phá ra là thời gian từ sóng R ở thất đến khi máy phát sốc chuyển nhịp (cardioversion) là 100 ms. Họ đòi phải đạt 50 ms thì mới an toàn. Mặc dù tất cả các báo cáo đều cho là an toàn (không tạo rung thất)
rung hai buồng đầu tiên của Cty Biotronik, máy Phylax AV. Ts Thống và một kỹ sư khác là tác giả chương trình Smart Detection phân biệt nguồn gớc các cơn loạn nhịp nhanh (thất hay trên thất) hiện vẫn còn được dùng chỉ với những thay đổi nhỏ so với chương trình nguyên thủy trong máy Phylax AV. Năm 1997, chương trình thiết kế máy Phylax AV đã kết thúc và Cty Biotronik sửa soạn xin cấp giấy phép lưu hành CE (Communauté Européenne). Các hoạt động thiết kế và phê chuẩn thiết kế (design validation) của nhóm kỹ sư ở Mỹ đã hoàn tất. Giai đoạn cuối cùng là phê chuẩn ở cấp Cty Biotronik. Ở giai đoạn này, các kỹ sư phê chuẩn thiết kế Đức tại Berlin khám phá ra là thời gian từ sóng R ở thất đến khi máy phát sốc chuyển nhịp (cardioversion) là 100 ms. Họ đòi phải đạt 50 ms thì mới an toàn. Mặc dù tất cả các báo cáo đều cho là an toàn (không tạo rung thất) nếu sốc được phát trước giữa sóng T, có nghĩa là sau 100 ms, nhóm phê chuẫn Đức nhất định là muốn đạt an toàn tối đa, phải đạt 50 ms. Vì quyết định này mà chứng nhận CE bị đình trễ 6 tháng để tái thiết kế máy. Điều quan trọng độc giả cần hiểu là trong cả thời gian này, GS Schaldach, ông chủ của Cty Biotronik, đã không can thiệp, vì đã giao quyên phê chuẩn thiết kế cho nhóm kỹ sư ở Berlin! Chúng tôi có bàn với các đồng nghiệp ở Mỹ và chúng tôi đều kết luận là chuyện đình trễ như vậy sẽ không bao giờ xảy ra ơ một Cty Mỹ (Medtronic, St Jude, Boston Scientific). Ở Mỹ, vì áp lực các cổ đông, các nhà điều hành công ty sẽ không bao giờ chấp nhận nhóm phê chuẩn thiết kế có nhiều quyền như vậy! Ở Mỹ, lịch trình (schedule) là tối quan trọng, nhất là khi chỉ vấp phải một vấn đề phụ!
nếu sốc được phát trước giữa sóng T, có nghĩa là sau 100 ms, nhóm phê chuẫn Đức nhất định là muốn đạt an toàn tối đa, phải đạt 50 ms. Vì quyết định này mà chứng nhận CE bị đình trễ 6 tháng để tái thiết kế máy. Điều quan trọng độc giả cần hiểu là trong cả thời gian này, GS Schaldach, ông chủ của Cty Biotronik, đã không can thiệp, vì đã giao quyên phê chuẩn thiết kế cho nhóm kỹ sư ở Berlin! Chúng tôi có bàn với các đồng nghiệp ở Mỹ và chúng tôi đều kết luận là chuyện đình trễ như vậy sẽ không bao giờ xảy ra ơ một Cty Mỹ (Medtronic, St Jude, Boston Scientific). Ở Mỹ, vì áp lực các cổ đông, các nhà điều hành công ty sẽ không bao giờ chấp nhận nhóm phê chuẩn thiết kế có nhiều quyền như vậy! Ở Mỹ, lịch trình (schedule) là tối quan trọng, nhất là khi chỉ vấp phải một vấn đề phụ! - Thế hệ dây điện cực sốc trước đây là dây Kentrox. Dây này có kích cở 9,3 French (1F= 1/3 mm). Cuối năm 2005, trong khi thiết kế dây Linox, thế hệ dây sau, nhóm kỹ sư thiết kế có thể đạt đường kính 7,8F và giử lớp
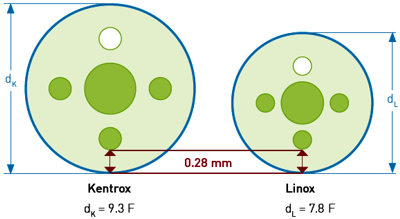 cách điện trong dây Linox dày bằng trong dây Kentrox, 0,28 mm (xem hình bên phải). Hoặc có thể giảm lớp cách điện bên ngoài và bên trong hầu có thể qua một ống thông 7F. Vào thời điểm đó Cty Medtronic có dây Sprint Fidelis có thể đưa qua ống thông 7F, được giới tim mạch khen là dây tốt
cách điện trong dây Linox dày bằng trong dây Kentrox, 0,28 mm (xem hình bên phải). Hoặc có thể giảm lớp cách điện bên ngoài và bên trong hầu có thể qua một ống thông 7F. Vào thời điểm đó Cty Medtronic có dây Sprint Fidelis có thể đưa qua ống thông 7F, được giới tim mạch khen là dây tốt  (bị recall, thu
(bị recall, thu
hồi,năm 2007 vì thiết kế không chuẩn ). Hình bên phải từ Bs Ip (MSU). Dây Riata (8F) đang được cung cấp vào thời điểm đó có lớp cách điện dày 0,09mm và 0,15 mm. Nếu dùng lớp cách điện như dây Riata, thì đường kính dây Linox có thể giảm 2x 0,19 mm, và dây Linox này sẽ đạt đường kính 6,7F, có thể qua ống thông 7F dễ dàng. Dây St Jude Riata đã lưu hành từ năm 2003 và được xem là một dây điện cực an toàn (nhưng đến năm 2010 thì bị ngưng cung cấp, và năm 2011 bị recall vì sự cố dây đồng lòi ra). Vì muốn đạt an toàn tối đa, nhóm thiết kế đã quyết định không thay đổi lớp cách điện bên ngoài, tiếp tục dùng lớp cách điện dày 0,28 mm. Ở một công ty Mỹ, chúng tôi chắc chắn là nhóm Marketing đã đòi hỏi các kỹ sự đạt đường kính <7F để có thể cạnh tranh với dây Sprint Fidelis 7F và dây Riata ST 7F sắp sửa được Cty St Jude giới thiệu (dây Riata ST bẳt đầu lưu hành năm 2006, cũng bị ngưng cung cấp năm 2010 và recall năm 2011, cùng với dây Riata).
Tóm lại truyền thống an toàn BN trên hết và truyền thống để các kỹ sư quyết định với sự góp ý của Marketing, thay vì truyền thống Marketing ở vị trí lãnh đạo như ở các công ty Mỹ, đã giúp Cty Biotronik đạt mức an toàn cao nhất trong các công ty máy tạo nhịp!
Do đó bạn có thể an tâm khi dùng các thiết bị Biotronik!
